ZVA: Apstrīdot "Rigvir" izplatīšanas aizliegumu, uzņēmums iesniedzis ar nereģistrētu metodi iegūtus testa rezultātus
Rīga, 21.maijs, LETA. Apstrīdot zāļu "Rigvir" izplatīšanas aizliegumu, šo zāļu reģistrācijas apliecības turētājs SIA "Latima" iesniedzis ar nereģistrētu metodi iegūtus testa rezultātus, aģentūra LETA uzzināja Zāļu valsts aģentūrā (ZVA).
Marta beigās Veselības inspekcijas (VI) un ZVA sadarbības rezultātā tika pieņemts lēmums apturēt "Rigvir šķīdums injekcijām" izplatīšanu līdz neatbilstības cēloņa noskaidrošanai un novēršanai. Pēc šī lēmuma pieņemšanas "Latima" vērsās VI ar vairākām sūdzībām, apstrīdot šo lēmumu un lūdzot nekavējoties to pārskatīt.
Kā norāda ZVA, izņēmuma kārtā "Latima" lūdza atļaut izplatīt vienu zāļu sēriju. Kopā ar sūdzībām un lūgumu "Latima" iesniedza testa rezultātus, kas iegūti Latvijas Infektoloģijas centra laboratorijā. Tomēr, pārskatot lēmumu un vērtējot to, vai zāļu "Rigvir" sēriju varētu atļaut izplatīt, inspekcija konstatēja, ka sūdzībām pievienotie testa rezultāti iegūti, izmantojot nereģistrētu testa metodi.
Šī iemesla dēļ VI secināja, ka testēšanas pārskati nepierāda zāļu "Rigvir" kvalitātes atbilstību prasībām un inspekcijai nav pamata grozīt lēmumu, kā arī atļaut izplatīt zāļu "Rigvir" sēriju.
VI arī informēja, ka maija sākumā tika saņemti 37 pacientu parakstīti iesniegumi ar lūgumu nekavējoties atcelt zāļu "Rigvir šķīdums injekcijām" izplatīšanas aizliegumu un atjaunot tā pieejamību. Vienlaikus inspekcija atgādināja, ka zāles "Rigvir" ir recepšu medikaments, kas izsniedzams tikai pret ārsta izrakstītu recepti.
Kā norāda iestādes, pagaidām neviena ārstniecības persona nav vērsusies inspekcijā vai ZVA ar lūgumu izņēmuma gadījumā atļaut izplatīt "Rigvir" pacientiem, kuri ar zālēm jau sākuši ārstēšanu.
Patlaban inspekcija sadarbībā ar ZVA iegūst informāciju, kas nepieciešama, lai lemtu, vai ārkārtas apstākļos pārejas periodā izņēmuma gadījumā var atļaut piegādāt vienu "Rigvir" sēriju pacientiem, kuri ar zālēm jau tiek ārstēti.
Abas iestādes sazinājušās arī ar Latvijas Onkologu asociāciju, kā arī ārstniecības iestādēm un ārstniecības personām, kas nodarbojas ar onkoloģisko pacientu ārstēšanu, ar lūgumu sniegt viedokli par nepieciešamību piemērot zāļu "Rigvir" izņēmumu, atļaujot veikt zāļu izplatīšanu.
ZVA uzskata, ka institūciju viedokļa uzklausīšana šajā jautājumā ir būtiska, lai iestādes varētu daudzpusīgi, savlaicīgi un informēti izvērtēt iespēju ārkārtas apstākļos pārejas periodā izņēmuma gadījumā atļaut izplatīt zāles "Rigvir".
VI informēšot sabiedrību par tās turpmāko rīcību un pieņemtajiem lēmumiem lietā par zālēm "Rigvir šķīdums injekcijām".
Jau vēstīts, ka saistībā ar konstatētām nepilnībām ZVA pieņēmusi lēmumu apturēt "Rigvir" izplatīšanu līdz neatbilstības cēloņa noskaidrošanai un novēršanai, turklāt Nacionālais veselības dienests (NVD) pieņēmis lēmumu par "Rigvir" svītrošanu no valsts Kompensējamo zāļu saraksta.
Lēmums saistīts ar to, ka ZVA saņēma Lielbritānijas oficiālās zāļu kvalitātes kontroles laboratorijas zāļu paraugu rutīnas testēšanas laikā veiktās zāļu "Rigvir" šķīdums injekcijām paraugu pārbaudes rezultātus, kuri liecina - "Rigvir" sastāvā ir mazāks vīrusa daudzums, nekā apstiprināts, šīs zāles reģistrējot.
Tā kā ZVA rīcībā nav informācijas par šo zāļu efektivitāti ar mazāku vīrusa daudzumu par reģistrācijas dokumentācijā norādīto minimālo daudzumu, pieņemts lēmums apturēt "Rigvir" izplatīšanu līdz neatbilstības cēloņa noskaidrošanai un novēršanai.
Vienlaikus ZVA informēja, ka "Latima" nav arī nodrošinājusi savlaicīgu aģentūras noteikto nosacījumu izpildi, tādēļ tiks lemts par medikamenta reģistrācijas apturēšanu.
Tikmēr pretvēža zāļu "Rigvir" ražotājs vērsies VI, lūdzot to steidzamības kārtā pārskatīt ZVA lēmumu par "Rigvir" izplatīšanas apturēšanu. Ražotājs VI lūdz piemērot pagaidu noregulējumu attiecībā uz vismaz vienu konkrētu "Rigvir" sēriju, kas pēc aiziešanas no Latvijas tirgus ir rezervēta Latvijas pacientiem, lai tie, kuri ir sākuši terapiju, varētu to turpināt, skaidroja uzņēmumā.
Patlaban NVD vērsies pie "Rigvir" zāļu reģistrācijas apliecības turētāja norādot, ka tā pienākums ir atlīdzināt nekvalitatīvo zāļu kompensēšanai izlietoto valsts finansējumu, bet ZVA informēja, ka saskaņā ar Zāļu izplatīšanas un kvalitātes kontroles kārtību reģistrācijas apliecības īpašniekam ir pienākums arī segt zaudējumus zāļu lieltirgotavām, aptiekām un citām personām, kurām zāles izplatītas ārpus kompensācijas sistēmas.
ZVA aicina - ja cilvēks līdz šim lietoja "Rigvir", būtu jāvēršas pie sava ārstējošā ārsta, lai saņemtu informāciju par turpmāko piemērotāko terapijas veidu.
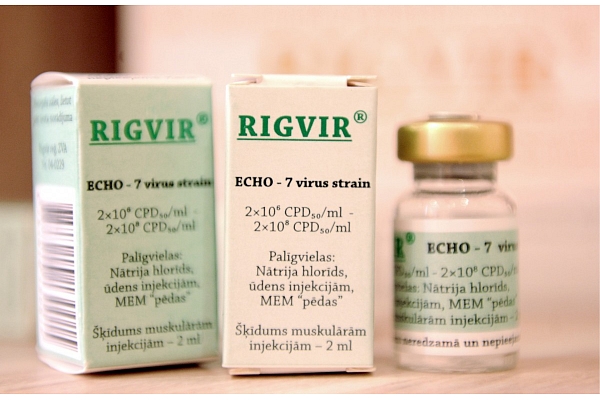
"Rigvir" ir vīrusu izcelsmes bioloģiskas zāles, kas paredzētas melanomas ārstēšanai. Saskaņā ar ZVA 2019.gada 18.martā saņemto SIA "Latima" vēstuli uzņēmums pēc savas iniciatīvas ir pieņēmis lēmumu uz laiku apturēt zāļu "Rigvir" izplatīšanu Latvijā, saglabājot spēkā esošo reģistrāciju.