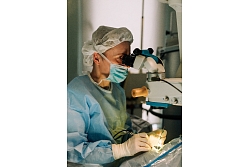
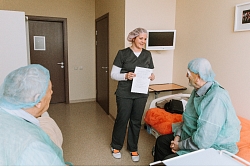
Zāļu klīniskie pētījumi organizēti augstā drošības līmenī
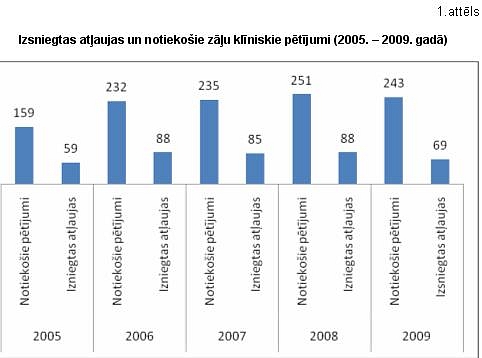
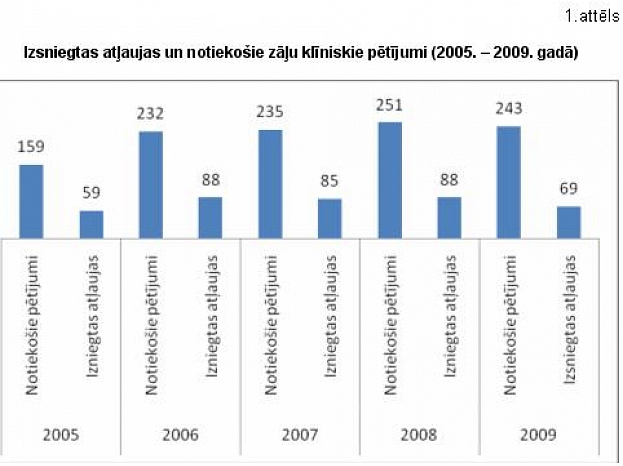
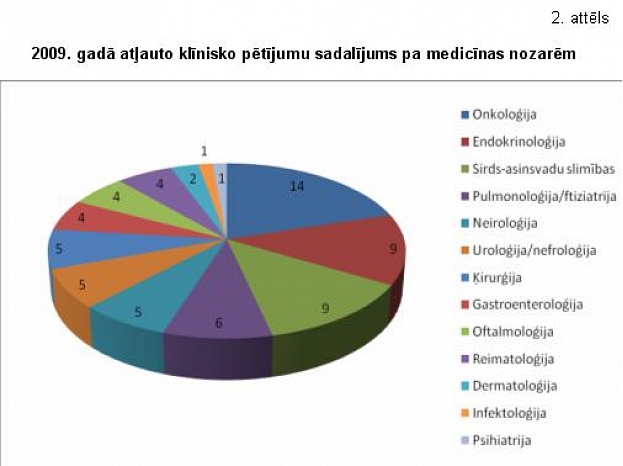
2009. gadā Latvijā norisinājušies 243 klīniskie pētījumi un izsniegtas atļaujas jauniem 69 pētījumiem (Skatīt. 1. un 2. attēlu.), tajā skaitā arī pētījumam ar Avandia, par kuru nesen medijos izskanējusi pretrunīga informācija.
2009. gada decembrī Zāļu valsts aģentūra ir izskatījusi un atļāvusi veikt pētījumu ar Avandia. Šis pētījums vienlaicīgi noris daudzās pasaules valstīs (t.sk. Zviedrijā, Dānijā, Nīderlandē, Vācijā, Īrijā, Somijā, Norvēģijā, Čehijā, Slovākijā, ASV, Kanādā), un pētījumā plānots kopā iesaistīt 16 000 pacientu. Pēc Aģentūrā esošās informācijas, pašlaik Latvijā pētījumā iesaistīti 9 pacienti.
Arī agrāk ar Avandia ir veikti klīniskie pētījumi. 2005.- 2008. gadā pētījumus vienlaicīgi veica vairākās valstīs, ieskaitot Rietumeiropas valstis un Latviju. Šo pētījumu laikā Zāļu valsts aģentūra nav saņēmusi nevienu ziņojumu par nāves gadījumiem, kas būtu tieši saistīti ar Avandia lietošanu.
Balstoties uz pētījumu datiem, 2008. gadā ES tika noteikts, ka zāles nedrīkst lietot atsevišķos sirds slimību gadījumos un tika atzīts, ka, lietojot zāles saskaņā ar norādījumiem zāļu aprakstā, guvums, ko sniedz šo zāļu lietošana atsver iespējamos riskus. Zāļu valsts aģentūra brīdināja veselības aprūpes speciālistus, ka Avandia nedrīkst lietot sirds slimnieki ar sirds mazspēju un slimnieki ar akūtu koronāro sindromu. Piesardzība zāļu lietošanā jāievēro cilvēkiem pēc 75 gadu vecuma.
Visās pasaules valstīs pastāv vienādas prasības attiecībā uz zāļu klīnisko pētījumu veikšanu. Pētījumā ar Avandia netiek iekļauti pacienti, kuriem, saskaņā ar Eiropas zāļu aģentūrā apstiprinātu zāļu aprakstu, ir aizliegts lietot šīs zāles. Pētījuma organizatora pienākums ir informēt pētījumā iesaistītos pacientus par jebkuru jaunu informāciju, kas varētu ietekmēt pacienta izvēli turpināt savu dalību šajā pētījumā. Kā arī pētījumā iesaistītais pacients jebkurā brīdi var pārtraukt savu dalību zāļu pētījumā. Klīniskajos pētījumos pacienti iesaistās labprātīgi, par dalību tajos netiek maksāts un pētījumi organizēti augstā drošības līmenī.
Atgādinām, ka Avandia ir Eiropas Savienībā (ES) centralizēti reģistrētas recepšu medikaments un tāpēc tas var tikt izplatīts visās ES dalībvalstīs.
Šogad Aģentūra saņēmusi 32 zāļu klīnisko pētījumu pieteikumus; līdz šim izsniegtas atļaujas 19 projektu uzsākšanai Latvijā. Pēdējos gados atļautajos pētījumos pārstāvēts plašs pētāmo zāļu spektrs: antibiotikas (t.sk., prettuberkulozes līdzekļi), antitrombotikie, pretaudzēju, antihipertensīvie, pretparkinsonisma, pretsāpju līdzekļi, kā arī līdzekļi izkaisītās sklerozes, obstruktīvās plaušu slimības ārstēšanai. Vairākos projektos tiek pētītas monoklonālās antivielas – rekombinētās DNS tehnoloģijās iegūtās zāles, ko izmanto reimatoīdā artrīta, psoriāzes un onkoloģisku saslimšanu ārstēšanā.
Pēc 2009. gada statistikas datiem populārākie zāļu klīnisko pētījumu centri ir P. Stradiņa Klīniskā universitātes slimnīca, Rīgas austrumu Klīniskā universitātes slimnīca, Vidzemes slimnīca un Daugavpils reģionālā slimnīca. Pērn pavisam pētījumi notikuši 64 ārstniecības iestādēs (pētījumu centros).
Viena no Zāļu valsts aģentūras funkcijām ir no zāļu ražotājiem vai to pārstāvjiem saņemto zāļu klīnisko pētījumu pieteikumu izvērtēšana un atļauju izsniegšana pētījumu uzsākšanai Latvijā. Aģentūra veic notiekošo zāļu klīnisko pētījumu uzraudzību un kontroli arī to norises laikā.
Sanita Skaidrā
Zāļu valsts aģentūras
Sabiedrisko attiecību speciāliste,